3차원 초음파를 이용한 태반 용적 및 혈관 지수 측정의 임상적 유용성: 전자간증 및 태아성장지연 예측이기수 (계명의대)
서론임신성 고혈압 질환과 태아성장지연(Fetal Growth Restriction, FGR)은 현대 산과학에서 주산기 예후를 결정짓는 핵심적인 합병증이다. 이러한 질환들의 공통적인 병태생리는 임신 초기 영양막 세포의 침윤 부전과 그에 따른 나선 동맥의 재형성 실패, 즉 태반 형성 부전(Placental Maldevelopment)에 기인한다(1). 기존의 2차원(2D) 초음파 검사는 태반의 위치나 두께, 에코 양상 등 정성적인 평가에는 유용했으나, 태반의 전체적인 용적이나 미세 혈류 역학을 정량적으로 분석하는 데에는 기술적 한계가 존재했다(2). 그러나 최근 3차원 초음파(3D Ultrasound) 및 3차원 에너지 도플러 초음파(3D Power Doppler Ultrasound, 3D-PDU) 기술의 발전으로 태반 용적(Placental Volume, PV)과 혈관 지수를 정밀하게 측정할 수 있게 되었으며, 이를 통해 질환의 발생을 조기에 예측하려는 연구들이 활발히 진행되고 있다(3). 전통적인 2D 초음파는 평면적인 단면만을 제공하기 때문에 태반과 같이 비정형적이고 입체적인 장기의 전체 크기를 측정하는 데 부적합하다. 2D 초음파를 이용한 태반 용적 추정은 대개 태반의 최대 두께나 단면적을 측정하여 기하학적 공식에 대입하는 방식을 취하지만, 이는 태반의 비대칭적인 성장을 반영하지 못한다. 3D 초음파는 태반의 전체 체적을 복수의 단면으로 획득하여 입체적으로 재구성함으로써 장기의 실제 기하학적 형태를 그대로 반영한다. 특히 에너지 도플러를 결합한 3D-PDU는 혈류의 방향이나 각도에 의존하지 않고 조직 내 적혈구의 밀도와 분포를 정량화할 수 있다는 점에서 2D 도플러와 차별화된다. 2D 도플러는 주로 자궁동맥(Uterine Artery)이나 제대동맥(Umbilical Artery)과 같은 대혈관의 저항 지수를 측정하여 간접적으로 태반 기능을 유추하지만, 3D-PDU는 태반 융모 간 공간(Intervillous Space) 내의 미세 혈관망 전체를 직접적으로 평가할 수 있는 능력을 갖추고 있다(3).3D 초음파 용적 측정의 주요 분석 방법론3D 초음파 데이터셋으로부터 태반 용적을 산출하기 위해서는 획득된 볼륨 데이터를 분석하는 소프트웨어 기법이 필요하다. 가장 근본적인 데이터 분석 방식인 Multiplanar 기법은 3차원 데이터를 가로(Axial), 세로(Sagittal), 관상면(Coronal)의 세 평면으로 분할하여 접근한다. 이 방식은 태반 전체를 일정하고 촘촘한 간격의 단면으로 잘라 각 단면의 면적을 구한 뒤 이를 합산하여 전체 부피를 구한다(4, 5). 수학적으로 가장 정교한 체적 계산이 가능하며 다른 분석 기법의 정확도를 평가하는 기준점이 되지만, 수백장에 달하는 모든 단면의 경계를 작업자가 직접 확인해야 하므로 분석 시간이 매우 오래 걸린다는 한계가 있다. 이러한 시간적 한계를 극복하기 위해 등장한 VOCAL(Virtual Organ Computer-aided Analysis) 기법은 회전축을 중심으로 데이터를 분석한다. 데이터 내에 중심축을 설정하고 이를 6도나 15도와 같은 일정 각도로 회전시키며 나타나는 단면에서 태반의 윤곽을 지정하는 방식이다(6). 6도 간격으로 분석할 경우 총 30개의 단면을 확인하게 되는데, 이는 태반처럼 자궁 벽을 따라 복잡한 곡선을 그리며 형성된 장기의 세밀한 경계를 추적하는데 효과적이다. 하지만 그럼에도 불구하고 30개의 단면을 평가하는 것은 현재의 임상 상황에서 실제 적용하기에는 너무 많은 시간이 걸린다고 볼 수 있다. XI VOCAL (eXtended Imaging VOCAL) 기법은 분석 속도를 더욱 높이기 위해 고정된 개수의 슬라이스 평면을 동시에 나열하여 부피를 계산한다. 미리 설정된 5개나 10개 등의 슬라이스 화면에서 경계를 지정하면 소프트웨어가 이를 연결하여 용적을 산출한다(4). 과정이 간편하고 속도가 빠르다는 이점이 있지만, 슬라이스 간격이 고정되어 있어 태반의 형태가 갑자기 변하거나 굴곡이 심한 부위의 데이터를 충분히 반영하지 못하는 정밀도의 한계를 보인다. 최근 초음파 기술은 인공지능(AI)과 딥러닝을 결합하며 분석을 패러다임을 바꾸고 있다. 수만개의 태반 영상 데이터를 학습한 딥러닝 모델을 기반으로 한 AI 기반 자동분석이 대표적인 예이다. 3D 볼륨 데이터가 입력되면 AI는 영상 내에서 태반 조직과 자궁 근층, 양수 등을 실시간으로 구분한다. 사람이 눈으로 경계를 찾기 힘든 모호한 부위도 AI는 픽셀 간의 명암 차이와 패턴을 분석하여 태반 영역을 확정한다. 그 후 식별된 태반 영역에 포함된 모든 복셀의 개수를 합산하여 즉각적으로 부피를 산출한다. 복셀은 3차원 공간에서 부피를 가진 최소 단위의 점을 의미하며, 이를 통해 계산하는 방식은 단면을 연결하는 기존 방식보다 공간적인 오차가 적고 정밀하다. AI 방식의 가장 큰 강점은 분석자의 숙련도나 주관에 관계없이 항상 동일하고 객관적인 결과값을 도출한다는 점이다. 사람이 직접 작업할 때 발생할 수 있는 피로도나 판단 오류를 배제할 수 있으며, 기존에 수 분이 소요되던 분석 시간을 단 몇 초 내외로 단축시켜 진료 현장에서 즉각적인 의사결정을 내릴 수 있게 한다.태반 혈관 지수의 정량화3D-PDU를 통해 얻을 수 있는 혈관 지수는 태반 내부의 혈류 역학을 수치화하여 제공한다. 이 지수들은 태반의 산소 및 영양분 전달 능력을 간접적으로 나타내는 지표로 활용된다(1). Vascularization Index(VI)는 관심 영역 내의 컬러 복셀(Color Voxel) 비율을 나타내며, 조직 내 혈관의 밀도를 반영한다. Flow Index(FI)는 컬러 신호의 평균 강도로, 혈관 내 적혈구의 이동 속도와 이동량을 반영한다. Vascularization Flow Index(VFI)는 VI와 FI를 결합한 복합 지수로, 전반적인 태반 관류 상태를 의미한다.질환 예측 모델에서의 활용전자간증은 태반의 관류 저하가 전신적인 모체 혈관 내피세포 손상으로 이어지는 질환이다. 3D-PDU 지수들은 자궁동맥 도플러보다 태반 내부의 관류 부전을 더 직접적으로 반영한다. 최근의 메타분석 결과에 따르면, VI, FI, VFI의 전자간증 예측 AUC(Area Under Curve)는 모두 0.89 내외로 매우 우수한 성적을 보였다(7). FGR은 태반의 기능적 용량이 태아의 유전적 성장 잠재력을 충족시키지 못할 때 발생한다. 태반용적은 임신 제1삼분기에 이미 정상군보다 작게 측정되는 경우가 많다. 3,500명의 임신부를 대상으로 한 연구에서 Z-score가 한 단위 감소할 때마다 FGR 발생 위험도가 1.736배 증가하는 것으로 나타났다(8).한계 및 미래 연구의 방향태반 분석이 임상에 완전히 정착하지 못한 데에는 몇 가지 현실적인 한계가 존재한다. 가장 큰 문제는 임신 주수가 진행됨에 따라 태반의 크기가 비대해 진다는 점이다. 임신 제1삼분기에는 태반이 한 화면에 모두 들어오기 때문에 전체 용적 측정이 용이하다. 그러나 임신 중기 이후부터는 태반이 자궁벽 전체로 넓게 퍼지며, 특히 전벽과 후벽에 걸쳐 있거나 자궁 기저부까지 넓게 분포하는 경우 3D 프로브의 최대 스캔 각도(보통 45°~90°)를 벗어나게 된다. 이 경우 전체 태반 용적을 구하지 못하고 일부분만 측정하게 되어 정확한 관류량을 산출하기 어렵다(9). 또한 도플러 신호는 초음파 기기의 설정 값(Gain, Pulse Repetition Frequency, Wall Filter 등)에 매우 민감하게 반응한다. 서로 다른 제조사의 기기를 사용하거나 사용자가 설정을 변경할 경우 지수 값이 달라질 수 있어, 전 세계적인 임상 표준을 확립하는 데 어려움이 있다. 또한 태반의 위치에 따라 초음파 감쇠(Attenuation) 정도가 달라져 지수 측정치에 편향이 발생할 수 있다. 현재 지목된 한계점들을 극복하기 위해 다양한 기술적 시도들이 이루어지고 있다. 특히 한 화면에 들어오지 않는 태반 문제를 해결하기 위한 영상 합성 기술과 분석 시간을 단축하기 위한 인공지능 기술이 핵심이다. 한 번의 스캔으로 담기 힘든 큰 태반을 측정하기 위해, 여러 개의 3D 볼륨 데이터를 획득한 후 이를 하나로 정교하게 이어 붙이는 '스티칭(Stitching)' 기술이 개발되었다(9). 적외선 카메라 트래킹 시스템을 통해 프로브의 정확한 공간 좌표를 파악하고, 자동으로 볼륨 데이터를 합성하여 전체 태반의 혈관망 모델을 구축하는 방식이다. 실험 결과에 따르면 이 방식은 92%의 재구성 성공률을 보였으며, 측정된 용적의 반복 재현성(ICC 0.96) 또한 매우 우수했다. 이는 중기 및 후기 임신에서도 태반 전체를 정량적으로 분석할 수 있는 길을 열어줄 것으로 기대된다. 일반적인 2D 프로브에 위치 추적 센서를 부착하여 복부를 훑으며 영상을 획득한 뒤, 이를 3D 볼륨으로 재구성하는 방식도 대안으로 제시되고 있다. 이 방식은 3D 프로브보다 유연하게 움직일 수 있어 음향 음영(Acoustic Shadow)을 피하기 쉽고, 태반의 전체적인 연장선을 따라 끊김 없는 데이터 획득이 가능하다(10). 또한 현재 분석의 가장 큰 장벽인 '수동 측정 시간'을 해결하기 위해 딥러닝 알고리즘이 도입되고 있다. OxNNet과 같은 완전 신경망(Fully Convolutional Neural Network) 모델은 수천 장의 초음파 데이터를 학습하여, 사람의 개입 없이 실시간으로 태반 영역을 인식하고 용적을 계산한다(11). AI 기반 자동 분할 기술은 관찰자 간 주관성을 배제하고, 분석 시간을 수 분에서 수 초 단위로 단축하여 진료 현장에서 즉각적인 위험도 산출을 가능하게 할 것이다(12). 3차원 초음파를 이용한 태반 용적 및 혈관 지수 측정은 전자간증과 태아성장지연의 조기 예측을 위한 강력한 도구이다. 비록 임신 후반부의 태반 비대화로 인한 기술적 제약과 표준화 문제가 여전히 남아 있으나, 이는 스티칭 기술과 인공지능의 결합을 통해 빠르게 극복되고 있다. 향후 자동화된 AI 분석 툴이 보편화되면, 태반 기능 평가는 단순한 연구 단계를 넘어 산전 관리의 필수적인 표준 검사로 자리 잡을 것이다.
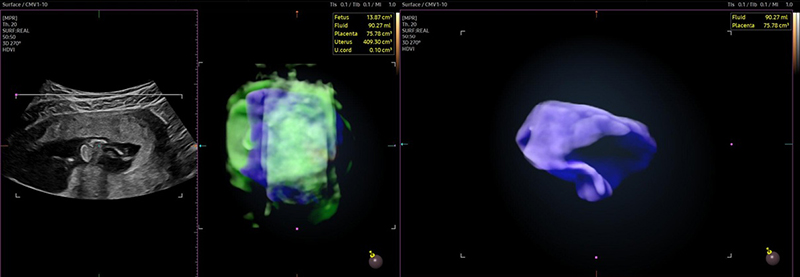
그림 1. 인공지능 기반 3차원 초음파를 이용한 태반 용적 자동 분할 및 정량화
좌) 3차원 초음파 영상에서 인공지능 딥러닝 알고리즘을 이용하여 태아, 양수, 자궁 및 태반을 자동 분할한 영상.
우) 자동 분할된 태반 영역만을 추출하여 3차원 재구성한 영상.
참고문헌
- Chen B, Chen H, Chen S, Chen Q, Wu S. Development and Validation of an Early-Pregnancy Prediction Model for Indicated Preterm Birth Using Three-Dimensional Placental Ultrasound and Maternal Clinical Characteristics. Int J Womens Health. 2026;18:555983.
- Odibo AO, Goetzinger KR, Huster KM, Christiansen JK, Odibo L, Tuuli MG. Placental volume and vascular flow assessed by 3D power Doppler and adverse pregnancy outcomes. Placenta. 2011;32(3):230–4.
- Wang Y, Liang L, Liu Y, Li P, Ren J. The Application Value of Three-Dimensional Power Doppler Ultrasound in Fetal Growth Restriction. Evid Based Complement Alternat Med. 2022;2022:4087406.
- Cheong KB, Leung KY, Li TK, Chan HY, Lee YP, Tang MH. Comparison of inter- and intraobserver agreement and reliability between three different types of placental volume measurement technique (XI VOCAL, VOCAL and multiplanar) and validity in the in-vitro setting. Ultrasound Obstet Gynecol. 2010;36(2):210–7.
- Nowak PM, Nardozza LM, Araujo Júnior E, Rolo LC, Moron AF. Comparison of placental volume in early pregnancy using multiplanar and VOCAL methods. Placenta. 2008;29(3):241–5.
- Larsen ML, Naver KV, Kjaer MM, Jorgensen FS, Nilas L. Reproducibility of 3-Dimensional Ultrasound Measurements of Placental Volume at Gestational Ages 11 - 14 Weeks. Facts Views Vis Obgyn. 2015;7(4):203–9.
- Wang Y, Zheng M, Bao M, Wang H. Assessment of uteroplacental perfusion with 3D power Doppler for the early prediction of pre-eclampsia: a systematic review and meta-analysis. Quant Imaging Med Surg. 2025;15(10):9765–77.
- Mathewlynn S, Starck LN, Wright D, Yin Y, Soltaninejad M, Nicolaides KH, et al. First-trimester Placental Ultrasound (FirstPLUS) study: prediction of fetal growth restriction using OxNNet-derived first-trimester placental volume. Ultrasound Obstet Gynecol. 2026;67(1):49–59.
- Xue A, Hanly R, Luichareonkit D, Thomas S, Barber T, Welsh AW. Automated multivolume placental reconstruction using three-dimensional power Doppler ultrasound and infrared camera tracking. Ultrasound Obstet Gynecol. 2025;65(5):624–32.
- Sagberg K, Lie T, H FP, Hillestad V, Eskild A, Bø LE. A new method for placental volume measurements using tracked 2D ultrasound and automatic image segmentation. Minim Invasive Ther Allied Technol. 2025;34(3):230–8.
- Schwartz N, Oguz I, Wang J, Pouch A, Yushkevich N, Parameshwaran S, et al. Fully Automated Placental Volume Quantification From 3D Ultrasound for Prediction of Small-for-Gestational-Age Infants. J Ultrasound Med. 2022;41(6):1509–24.
- Looney P, Stevenson GN, Nicolaides KH, Plasencia W, Molloholli M, Natsis S, et al. Fully automated, real-time 3D ultrasound segmentation to estimate first trimester placental volume using deep learning. JCI Insight. 2018;3(11).



 로그인
로그인 회원가입
회원가입 ENG
ENG
 이메일 무단 수집 거부
이메일 무단 수집 거부